“Hympavz”--首款FDA批準的TFPI抗體,血友病治療新突破!
日期:2024-12-02 10:19:00
近期,輝瑞公司宣布其TFPI抗體Marstacimab(商品名Hympavzi,中文名馬塔西單抗)獲得FDA批準上市,標志著血友病治療領域的一大進步。Hympavzi作為首款FDA批準的TFPI抗體,不僅為A型和B型血友病成人及12歲以上兒童患者提供了一種新的預防和降低出血發作頻率的治療選擇,還因其便捷的自我給藥方式,極大地提高了患者的生活質量。通過靶向TFPI的Kunitz-2結構域,Hympavzi能夠阻斷TFPI的活性,抑制外源性凝血途徑,從而重新建立出血和凝血之間的平衡 [1]。TFPI作為血漿中一種新近發現的抗凝蛋白,其作用是通過抑制FXa和FVIIa-TF發揮抗凝作用,這一機制的發現和應用,為血友病的治療提供了新的思路,也為未來凝血機制研究和新藥開發提供了重要的科學基礎。目前,多款TFPI靶向藥正在涌現,有望帶來更多創新療法,改善血友病患者的治療效果和生活質量,為患者帶來更便捷、更有效的治療方案!
1. 什么是TFPI?
組織因子途徑抑制物(Tissue Factor Pathway Inhibitor,TFPI)是一種體內天然抗凝蛋白,它對組織因子途徑(即外源性凝血途徑)具有特異性抑制作用。結構上,TFPI為單鏈糖蛋白,屬于Kunitz型絲氨酸蛋白酶抑制劑家族,其結構特征是存在三個串聯的Kunitz型抑制功能域,從N端到C端分別稱為K1,K2,K3。其中,Kunitz1能與FVIIa-TF復合物結合,Kunitz2能與FXa結合,但Kunitz3的意義尚未明確(圖1) [1]。一般而言,TFPI在體內可大體分為三個池:①血管內皮細胞的TFPI大部分結合于內皮細胞表面,肝素可以刺激它的釋放;②血小板的TFPI在凝血酶的刺激下可釋放出來,與局部凝血過程的控制有關;③血漿中的TFPI大部分與脂蛋白結合 [2]。
生理情況下,TFPI主要錨著于血管內皮細胞,TFPI的恒定表達對內皮細胞的抗凝血功能及維持血液的正常流動非常重要。TFPI作為目前唯一能生理性抑制TF啟動的外源性凝血途徑的一種內源性抗凝蛋白,對TF誘導的凝血具有抑制調節作用,在白血病、心血管等疾病中發揮重要作用。那么TF是什么?TFPI又是如何發揮抗凝血作用?
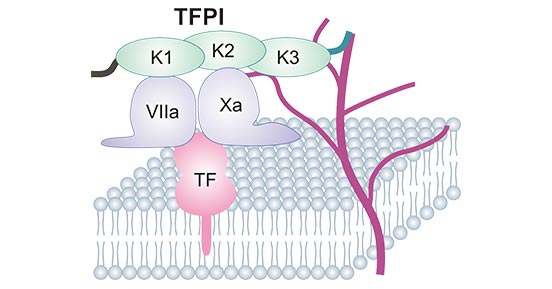
圖1. TFPI三個串聯的Kunitz結構
2. 什么是TF?
組織因子(Tissue Factor,TF)是公認的機體內最強的促凝血因子之一,是生理止血的凝血過程和病理血栓形成的啟動環節。成熟的TF分子主要由胞外區、跨膜區和胞內區組成,其中,TF分子的胞外區是與凝血因子VII(FVII)或活化凝血因子(FVIIa)相結合并激發凝血的關鍵部位,具有促凝血活性 [3]。
在病理情況下,TF與血液中高親和力的凝血因子VII(FVII)結合,迅速轉為活化的凝血因子VIIa(FVIIa),形成FVIIa-TF活性復合物聚集在細胞表面,當在磷脂和Ca2+存在時,FVIIa-TF又迅速激活酶原(FX),形成FXa。生成的FXa又能反過來激活FVII,可使更多FX激活,形成外源性凝血途徑的正反饋效應。TF還能以較低的速度激活FIX,在局部生成大量凝血酶,出現血液凝固。因此,TF可同時激活內、外源凝血途徑 (圖2)[4, 5]。
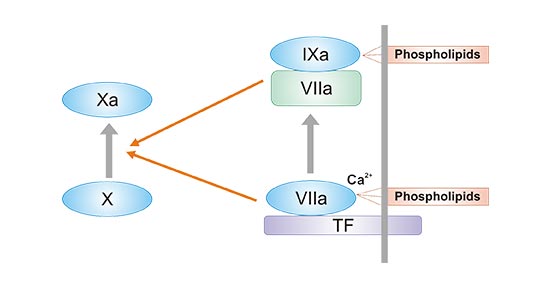
圖2. TF激活內外凝血途徑示意圖
3. TFPI抑制TF凝血作用機制
TFPI對TF凝血抑制作用屬于負反饋性質。在病理情況下(如內皮細胞嚴重受損、感染時均可刺激血管內皮細胞表達TFPI),TF表達并與血漿中的FVII或FVIIa結合激活外源性凝血途徑。
TFPI對TF凝血途徑的抑制主要分以下進行:首先,TFPI通過K2與FXa結合,并競爭性抑制其催化活性,進而改變自身結構,該過程是一個Ca2+非依賴的可逆性過程;然后,FXa-TFPI復合物中的TFPI通過K1與FVIIa-TF復合物中的FVIIa活性部位相結合,從而實現對FVIIa-TF復合物的抑制。FXa輕鏈中谷氨酸殘基上的γ-羧基與Ca2+結合,并通過“鈣橋(Calcium Bridging)”結合于FXa-FVIIa-TF復合物中TF附近的磷脂表面,使得FXa-TFPI與FVIIa-TF形成穩固的FVIIa-TF-FXa-TFPI四元復合物,滅活FVIIa-TF復合物,抑制外源性凝血途徑。因此,只有凝血途徑途徑啟動后,TFPI才會發揮它的抑制凝血作用,從而調節TF的促凝活性。高濃度的TFPI在FXa缺乏的條件下可作為FVIIa-TF復合物的唯一生理抑制劑,抑制FVIIa-TF的活性,在外源性凝血途徑中發揮重要作用 [6] (圖3)。

圖3. TFPI抗凝血作用機制
4. TFPI在血友病、心血管疾病及腫瘤中的作用
● TFPI與血友病
血友病屬于一種單基因的X連鎖隱性疾病,其主要特征是出現活性凝血活酶生成障礙,也就是凝血因子缺乏導致的遺傳性出血性疾病,常表現為自發性出血或輕度外傷后出血不止。根據缺乏的凝血因子的種類不同,血友病主要分為血友病A和血友病B兩類,分別為凝血因子VIII和凝血因子IX缺乏所致。臨床上血友病A最常見,占比約80%-85% [7]。
如前所述,FVIIa-TF可以直接激活FX成為FXa。然而,TFPI可以滅活FXa與FVIIa-TF,所以,在生理止血的凝血過程中,組織因子TF的途徑作用是短暫的。凝血過程的維持與完成有賴于內在途徑的存在,這也是血友病(乏FVⅢ、乏FIX、乏FXI)發生凝血障礙的主要原因。目前,凝血因子替代療法是血友病患者的主要治療手段,但是很多患者在接受治療過程中會產生凝血因子的抑制劑(免疫系統產生的抗體),從而影響治療效果。若設法消除TFPI的作用,則組織因子TF途徑的作用,就不再是短暫的,而能將凝血過程完成。在采用家兔型血友病模型中,應用rTFPI抗體抑制TFPI,可使兔出血時間明顯縮短,這為血友病治療提供了一個新的途徑 [8, 9]。
● TFPI與心血管疾病
正常情況下,血管內皮細胞不表達TF,但多種心腦血管疾病,如心絞痛、冠狀動脈或腦動脈粥樣硬化等疾病狀態下,因血管內皮細胞受損,引起內皮細胞功能紊亂而表達TF。研究發現,當發生動脈粥樣硬化時,單核/巨噬細胞中的TF暴露在血循環中,具有促凝活性,誘導血栓發生。但TFPI可抑制TF,改善并發癥,調節血栓形成。此外,在心肌梗塞,冠狀動脈局部缺血,動脈粥樣硬化等疾病中,血漿TFPI水平增高,提示TFPI可以調節TF的活性,在抑制血栓形成和血管重塑等方面發揮重要作用 [10, 11]。
● TFPI與腫瘤
近年來,研究人員發現凝血過程參與因子在腫瘤的發生、發展過程中常伴有異常表達。目前,TFPI在惡性腫瘤中的表達水平意見尚不一致。一方面,癌細胞和白血病原始細胞產生的IL-11和TNFa,可刺激TFPI的合成。另一方面,TFPI也屬于抗血管腫瘤新生因子之一,意味著TFPI也可能通過調節血管生成抑制腫瘤生長。目前認為,TFPI對抗腫瘤可能主要有兩種途徑:①抑制FVIIa-TF活性。TF可促進血管新生、細胞遷移、細胞黏附和上調腫瘤細胞增殖。因此,TFPI可調節TF活性,抑制腫瘤 (圖4);②TFPI通過與VLDL受體(極低密度脂蛋白受體)相互作用對抗血管新生、細胞增殖、腫瘤生長 [13, 14]。

圖4. TFPI抑制FVIIa-TF活性對抗腫瘤
5. TFPI臨床研究前景
來自Pharmsnap的數據庫顯示(表1),多項針對TFPI靶點的藥物研發正積極進行,主要聚焦于單克隆抗體類藥物,其在血友病治療領域取得了顯著進展,并有潛力擴展至膿毒癥、炎癥性疾病和心血管疾病等其他領域。輝瑞的馬塔西單抗(Marstacimab)作為一種人源IgG1單克隆抗體,已在2024年10月15日獲得FDA批準,用于12歲以上的血友病A或B患者。此外,諾和諾德的康賽珠單抗(Concizumab),另一種靶向TFPI Kunitz-2結構域的藥物,曾獲得日本藥監局批準,但在FDA審批過程中因血栓事件被拒,這同時也突顯了新藥研發中安全性監控和評估的重要性。蘇州康寧杰瑞的KN057(Armocibart),作為國內首個抗TFPI單抗,已進入III期臨床研究階段,通過中和TFPI對FXa及TF/FVIIa復合物的抑制作用來維持凝血酶水平,預防出血,適用于伴或不伴抑制物的A型與B型血友病患者。總之,這些藥物不僅為血友病患者提供了新的治療選擇,尤其是對傳統療法產生抑制物或療效不佳的患者具有重要意義。隨著研究的深入,預計TFPI藥物將拓展到更多治療領域,進一步擴大其市場潛力!
| 藥物 | 靶點 | 藥物類型 | 在研適應癥(疾病名) | 在研機構 | 最高研發階段 |
|---|---|---|---|---|---|
| 馬塔西單抗 | TFPI | 單克隆抗體 | 血友病A | 血友病B | 血友病 | Pfizer Inc. | 輝瑞投資有限公司 | Pfizer Europe MA EEIG | 批準上市 |
| 康賽珠單抗 | TFPI | 單克隆抗體 | 血友病A | 血友病B | Novo Nordisk A/S | Novo Nordisk Canada, Inc. | Novo Nordisk Pharma Ltd. | Novo Nordisk Pharmaceuticals Pty Ltd. | 批準上市 |
| Armocibart | TFPI | 單克隆抗體 | 血友病A | 血友病B | 馮·維勒布蘭德病 | 蘇州康寧杰瑞生物科技有限公司 | 臨床3期 |
| ZED-1227 | TFPI | 合成多肽 | 肝纖維化 | 代謝功能障礙相關的脂肪肝病 | 乳糜瀉 | Dr. Falk Pharma GmbH | Takeda Pharmaceutical Co., Ltd. | Zedira GmbH | 臨床2期 |
| MG-1113 | TFPI | 單克隆抗體 | 血友病A | 血友病B | GC Biopharma Corp. | 臨床1期 |
| Anti-TPFI neutralizing mAb gene therapy (Pfizer) | TFPI | 腺相關病毒基因治療 | 血友病A | Pfizer Inc. | 臨床前 |
| DN-201782 | TFPI | 小分子化藥 | 腎細胞癌 | Daegu-Gyeongbuk Medical Innovation Foundation | 臨床前 |
| JTP-96193 | TFPI | 小分子化藥 | 2型糖尿病 | Japan Tobacco, Inc. | 臨床前 |
| 替法可近 | F10 x TFPI x factor VII | 小分子化藥 | 膿毒性休克 | Chiron Corp. | 臨床前 |
| WO2023241389 | TFPI | 單克隆抗體 | 血液及淋巴系統疾病 | 安源醫藥科技(上海)有限公司 | 藥物發現 |
| WO2024143987 | TFPI | 單克隆抗體 | 皮膚和肌肉骨骼疾病 | Green Cross Holdings Co., Ltd. | Green Cross Co., Ltd. | 藥物發現 |
表1. TFPI在研臨床研究藥物
為鼎力協助各藥企針對TFPI靶點在血友病、心血管疾病以及腫瘤等藥物方面的研發工作,CUSABIO推出TFPI活性蛋白產品(Code: CSB-MP023437HU;Code: CSB-MP023437RB),助力您在TFPI機制方面的研究或其潛在臨床價值的探索。
● Recombinant Human Tissue factor pathway inhibitor(TFPI),partial (Active)
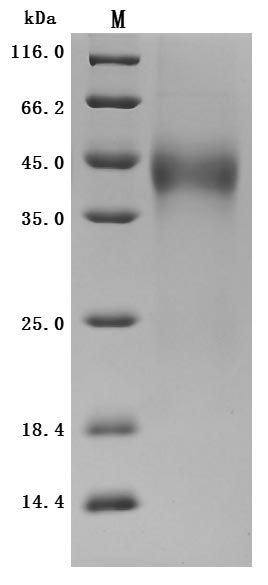
Purity was greater than 95% as determined by SDS-PAGE. (Tris-Glycine gel) Discontinuous SDS-PAGE (reduced) with 5% enrichment gel and 15% separation gel.
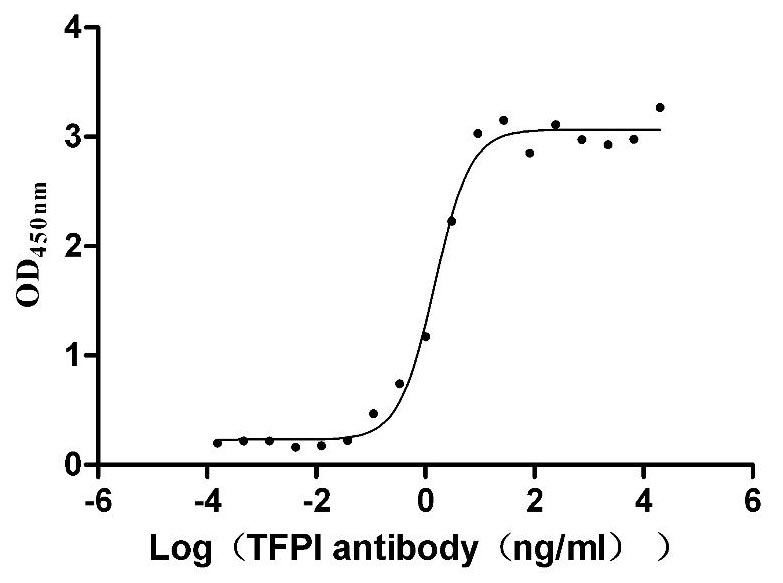
Immobilized Human TFPI at 1 μg/ml can bind Anti-TFPI recombinant antibody (CSB-RA023437MA01HU), the EC50 is 1.242-1.788 ng/mL.
● Recombinant Rabbit Tissue factor pathway inhibitor(TFPI) (Active)

Purity was greater than 95% as determined by SDS-PAGE. (Tris-Glycine gel) Discontinuous SDS-PAGE (reduced) with 5% enrichment gel and 15% separation gel.
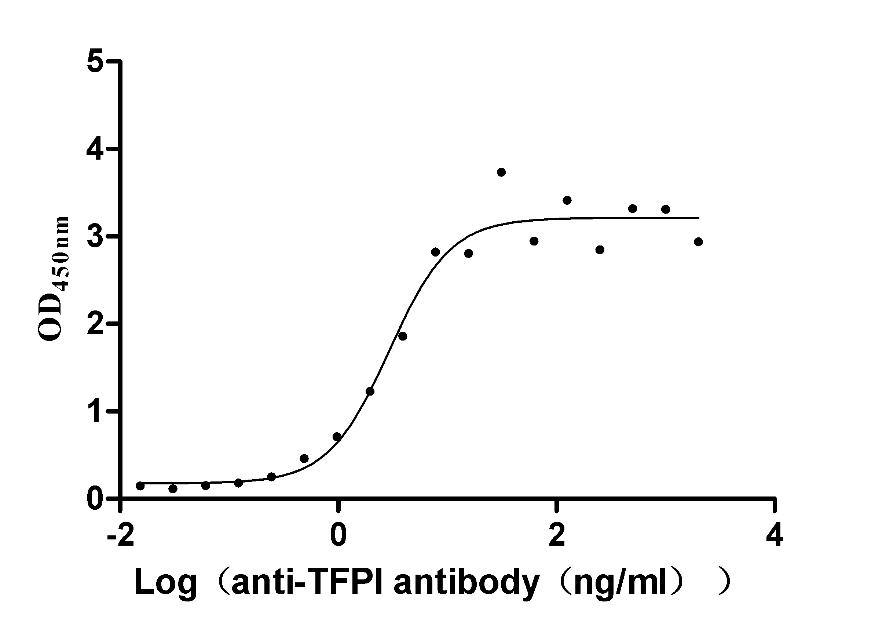
Immobilized Rabbit TFPI at 1 μg/ml can bind Anti-TFPI recombinant antibody (CSB-RA023437MA01HU), the EC50 is 2.281-3.783 ng/mL.
參考文獻:
[1] https://www.pfizer.com/news/press-release/press-release-detail/us-fda-approves-pfizers-hympavzitm-marstacimab-hncq
[2] Kato, Hisao. "Regulation of functions of vascular wall cells by tissue factor pathway inhibitor: basic and clinical aspects." Arteriosclerosis, thrombosis, and vascular biology 22.4 (2002): 539-548.
[3] Lin, C. C., et al. "Atorvastatin or transgenic expression of TFPI inhibits coagulation initiated by anti-nonGal IgG binding to porcine aortic endothelial cells." Journal of Thrombosis and Haemostasis 8.9 (2010): 2001-2010.
[4] Mackman, Nigel, Steven P. Grover, and Silvio Antoniak. "Tissue factor expression, extracellular vesicles, and thrombosis after infection with the respiratory viruses influenza A virus and coronavirus." Journal of Thrombosis and Haemostasis 19.11 (2021): 2652-2658.
[5] D'Angelo, G. "Inflammation and coagulation: a "continuum" between coagulation activation and prothrombotic state." j Blood Disord 2.1 (2015): 1023.
[6] Østerud, Bjarne. "Tissue factor/TFPI and blood cells." Thrombosis research 129.3 (2012): 274-278.
[7] Gomez, Keith, and John H. McVey. "Tissue factor initiated blood coagulation." Front Biosci 11.1 (2006): 1349-59.
[8] Alblaihed, Leen, et al. "High risk and low prevalence diseases: Hemophilia emergencies." The American Journal of Emergency Medicine (2022).
[9] Adams, Murray. "Tissue factor pathway inhibitor: new insights into an old inhibitor." Seminars in thrombosis and hemostasis. vol. 38. no. 02. Thieme Medical Publishers, 2012.
[10] Price, G. C., S. A. Thompson, and P. C. A. Kam. "Tissue factor and tissue factor pathway inhibitor." Anaesthesia 59.5 (2004): 483-492.
[11] Naji, Duraid Hamid, et al. "Significant genetic association of a functional TFPI variant with circulating fibrinogen levels and coronary artery disease." Molecular genetics and genomics 293.1 (2018): 119-128.
[12] Jude, B., et al. "Relevance of tissue factor in cardiovascular disease." Archives des Maladies du Coeur et des Vaisseaux 98.6 (2005): 667-671.
[13] Tinholt, Mari, et al. "Tumor expression, plasma levels and genetic polymorphisms of the coagulation inhibitor TFPI are associated with clinicopathological parameters and survival in breast cancer, in contrast to the coagulation initiator TF." Breast Cancer Research 17.1 (2015): 1-15.
[14] Lopez-Pedrera, C., et al. "Tissue factor as an effector of angiogenesis and tumor progression in hematological malignancies." Leukemia 20.8 (2006): 1331-1340.
[15] Hembrough, Todd A., et al. "Identification and characterization of a very low density lipoprotein receptor-binding peptide from tissue factor pathway inhibitor that has antitumor and antiangiogenic activity." Blood 103.9 (2004): 3374-3380.










