SEZ6:神經內分泌腫瘤治療新靶點,多款ADC臨床在研
日期:2025-07-25 09:52:46
1. SEZ6背景介紹
Seizure-related 6 homolog(癲癇相關同源物6,SEZ6)是一種跨膜蛋白,最初因與癲癇相關而被發現 [1]。其基因定位于染色體 17q21.33,編碼的蛋白包含多個結構域,在神經系統中具有重要作用。
SEZ6的表達具有組織特異性。在正常組織中,SEZ6主要在腦(如小腦、大腦、脊髓)和垂體中表達,而在其他組織(如肺、肝、腎等)中表達量極低 [2,3]。RNA測序和免疫組織化學(IHC)分析顯示,SEZ6在小細胞肺癌(SCLC)、神經內分泌癌(NECs)等神經內分泌腫瘤中高表達,且與神經內分泌標志物chromogranin A(CHGA)的表達高度相關 [2]。在73例原發性SCLC樣本中,約78%的腫瘤存在SEZ6陽性表達,平均陽性率為40.4%,表明其在SCLC中具有較高的 prevalence [2]。
此外,SEZ6在小鼠內耳的神經感覺毛細胞中也有表達,且在胚胎、出生后及成年階段均持續存在,提示其在聽覺系統發育和功能維持中可能發揮作用 [3]。
2. SEZ6研究機制
SEZ6是β- 分泌酶(BACE1)的重要底物。BACE1可切割SEZ6的胞外域,產生可溶性ectodomain(sSEZ6)和跨膜C端片段(SEZ6-CTF);隨后,SEZ6-CTF可被γ-分泌酶進一步切割,釋放胞內域(SEZ6-ICD)[4]。這一切割過程在神經元中高度特異性發生,且對SEZ6的功能至關重要。
在SCLC中,SEZ6作為細胞表面蛋白,可被特異性抗體(如 SC17)識別并誘導快速內化,這一特性使其成為抗體-藥物偶聯物(ADC)的理想靶點 [2]。研究顯示,靶向SEZ6的ADC(如 ABBV-011)可通過內化進入腫瘤細胞,釋放細胞毒性payload(如 calicheamicin),從而特異性殺傷SEZ6陽性腫瘤細胞 [2]。
3. SEZ6相關信號通路
3.1 BACE1-SEZ6-γ-secretase通路
該通路是SEZ6最核心的信號通路。BACE1切割SEZ6產生的SEZ6-CTF可通過結合ERM蛋白傳遞信號,調控細胞骨架重組(如生長錐塌陷);而γ-分泌酶對SEZ6-CTF的進一步切割則可終止該信號,使細胞恢復對新信號的響應能力 [4]。在神經元中,這一通路參與軸突導向和突觸可塑性調節 [4]。
3.2 與神經內分泌信號的關聯
在SCLC中,SEZ6的表達與CHGA等神經內分泌標志物高度相關 [2],提示其可能參與ASCL1(一種驅動神經內分泌細胞命運的轉錄因子)調控的信號通路。研究顯示,SEZ6是ASCL1的下游靶基因,在ASCL1高表達的SCLC亞型中顯著上調 [2]。
3.3 聽覺信號通路
在小鼠內耳中,SEZ6在毛細胞的stereocilia和胞質中表達,可能通過調控離子通道(如鉀通道)參與聽覺信號的傳遞與整合 [3]。其突變可能影響毛細胞的結構和功能,導致聽力障礙。
4. SEZ6相關疾病
4.1 腫瘤
4.1.1 小細胞肺癌(SCLC)
SEZ6在SCLC中高表達,且與不良預后相關——高SEZ6表達的SCLC患者生存期更短 [2]。機制上,SEZ6可能通過與ezrin-radixin-moesin(ERM)家族蛋白相互作用,影響腫瘤細胞的骨架動態,從而促進腫瘤生長和侵襲 [2,3]。基于其高特異性和內化特性,靶向SEZ6的ADC(如 ABBV-011、ABBV-706)已進入臨床試驗,用于治療復發/難治性 SCLC [2,6]。
4.1.2 神經內分泌癌(NECs)
SEZ6在NECs中同樣高表達,是潛在的治療靶點,相關聯合治療(如與 PD-1 抑制劑、鉑類藥物聯用)正在研究中 [6]。
4.2 聽力障礙
SEZ6 的純合錯義突變(如 c.2092G>A:p.Val698Ile)與常染色體隱性非綜合征性聽力障礙相關。在巴基斯坦近親家系中,該突變導致SEZ6蛋白結構異常,影響內耳毛細胞功能,表現為先天性重度感音神經性耳聾 [3]。SEZ6在小鼠內耳的神經感覺毛細胞中表達,且在胚胎、出生后及成年階段均持續存在,提示其在聽覺系統發育和功能維持中發揮作用 [3]。
4.3 神經系統疾病
4.3.1 癲癇
SEZ6最初因與癲癇相關而被命名,其表達異常可能通過影響神經元興奮性參與癲癇發作 [1,7]。
4.3.2 阿爾茨海默病(AD)
SEZ6是BACE1的底物,而BACE1是AD中Aβ產生的關鍵酶。BACE1抑制劑可減少SEZ6的切割,導致突觸可塑性受損(如 LTP 降低),提示SEZ6可能參與AD的突觸功能障礙 [4,8]。SEZ6敲除小鼠的皮質錐體細胞樹突分支減少,興奮性異常,海馬區樹突棘密度降低,導致空間記憶缺陷 [4]。
4.3.3 認知與行為異常
SEZ6敲除小鼠表現出認知缺陷、運動協調障礙和情緒反應異常,與人類的智力障礙和精神分裂癥表型相關)[4]。SEZ6通過調控kainate受體亞基GluK2和GluK3的糖基化與運輸,影響突觸傳遞 [3],這可能是其導致認知異常的機制之一。
5. SEZ6靶點藥物研究進展
SEZ6在正常組織中低表達、但在神經內分泌腫瘤(如小細胞肺癌SCLC)中高表達,因此成為抗體偶聯藥物(ADC)的熱門靶點。目前已有多條ADC管線在研,適應癥以小細胞肺癌為主,最高研發階段臨床1期。部分在研管線列舉如下:
| 藥物 | 作用機制 | 藥物類型 | 在研適應癥(疾病名) | 在研機構 | 最高研發階段 |
|---|---|---|---|---|---|
| SC-011 | DNA抑制劑 | SEZ6抑制劑 | ADC | 難治性小細胞肺癌 | AbbVie, Inc. | 臨床1期 |
| ABBV-706 | SEZ6抑制劑 | TOP1抑制劑 | ADC | 晚期惡性實體瘤 | 小細胞肺癌 | 復發性小細胞肺癌 | 難治性小細胞肺癌 | 非小細胞肺癌 | AbbVie, Inc. | 臨床1期 |
| DLL3xSEZ6 bsADC(Biocytogen) | DLL3抑制劑 | SEZ6抑制劑 | TOP1抑制劑 | ADC | 小細胞肺癌 | Biocytogen Boston Corp. | 臨床前 |
| DEC-002 | SEZ6抑制劑 | ADC | 腫瘤 | 無錫藥明生物技術股份有限公司 | Whitehawk Therapeutics, Inc. | 杭州多禧生物科技有限公司 | 臨床前 |
| HWK-206 | SEZ6調節劑 | ADC | 神經內分泌癌 | 小細胞肺癌 | Whitehawk Therapeutics, Inc. | 臨床前 |
(數據來源于Patsnap)
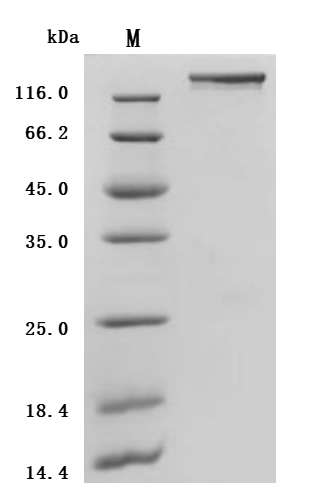
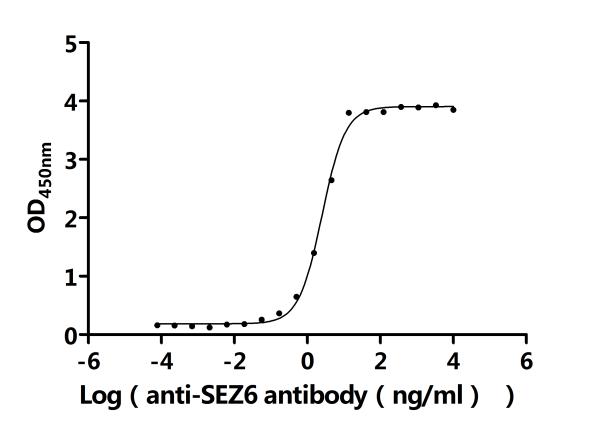
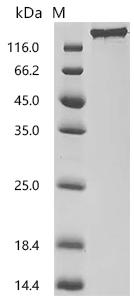
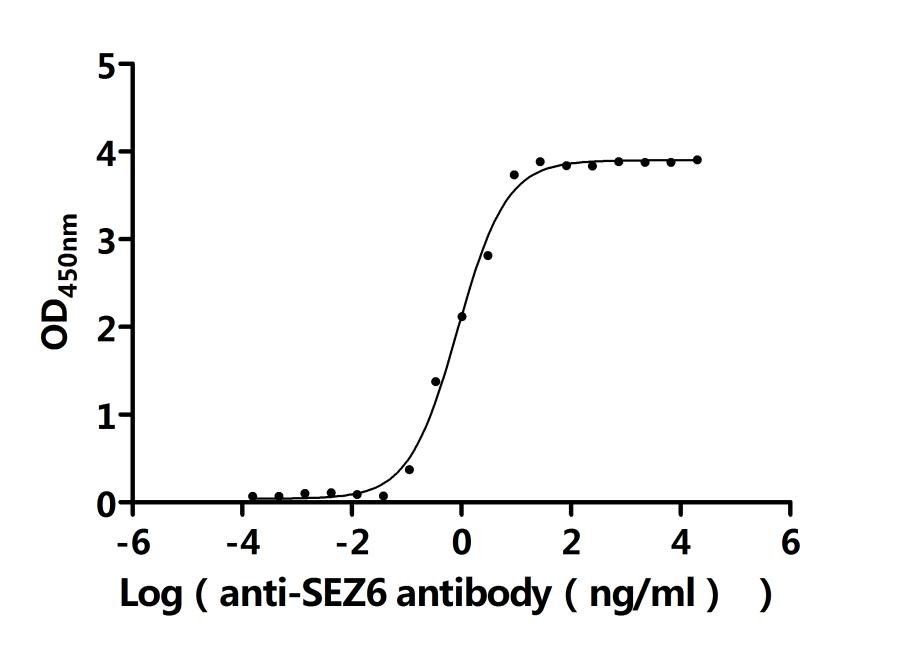
6. 華美生物SEZ6研究相關產品推薦
參考文獻:
[1] Gunnersen JM, Kim MH, Fuller SJ, et al. Sez-6 proteins affect dendritic arborization patterns and excitability of cortical pyramidal neurons. Neuron, 2007, 56: 621-639.
[2] Wiedemeyer WR, Gavrilyuk J, Schammel A, et al. ABBV-011, A Novel, Calicheamicin-Based Antibody–Drug Conjugate, Targets SEZ6 to Eradicate Small Cell Lung Cancer Tumors. Molecular Cancer Therapeutics, 2022, 21(6): 986-998.
[3] Bharadwaj T, Schrauwen I, Rehman S, et al. ADAMTS1, MPDZ, MVD, and SEZ6: candidate genes for autosomal recessive nonsyndromic hearing impairment. European Journal of Human Genetics, 2022, 30: 22-33.
[4] Shimizu-Nishikawa K, Kajiwara K, Kimura M, et al. Cloning and expression of SEZ-6, a brain-specific and seizure-related cDNA. Brain Res Mol Brain Res, 1995, 28: 201-210.
[5] Ohno M, Sametsky EA, Younkin LH, et al. BACE1 deficiency rescues memory deficits and cholinergic dysfunction in a mouse model of Alzheimer's disease. Neuron, 2004, 41: 27-33.
[6] Chandana S, Garmezy B, Dowlati A, et al. Phase I study of ABBV-706, an anti-SEZ6 antibody-drug conjugate, alone or in combination in adults with advanced solid tumors. Annals of Oncology, 2023, 34(S2): S1077.
[7] Pigoni M, Hsia HE, Hartmann J, et al. Seizure protein 6 controls glycosylation and trafficking of kainate receptor subunits GluK2 and GluK3. EMBO J, 2020, 39: e103457.
[8] Zhu K, Xiang X, Filser S, et al. BACE1 Inhibition Impairs Synaptic Plasticity via Seizure Protein 6. Biological Psychiatry, 2017, doi:10.1016/j.biopsych.2016.12.023.