前沿靶點(diǎn)速遞:每周醫(yī)學(xué)研究精選(十六)
日期:2024-10-23 13:05:43
靶點(diǎn):Plin2
應(yīng)用:脂肪肝病的治療研究
來(lái)源:Wang, Yao, et al. "Therapeutic siRNA targeting PLIN2 ameliorates steatosis, inflammation, and fibrosis in steatotic liver disease models." Journal of Lipid Research 65.10 (2024): 100635.

北京大學(xué)生命科學(xué)學(xué)院朱健和劉敏課題組在《Journal of Lipid Research》上發(fā)表的研究論文中,報(bào)道了一種靶向治療脂肪肝病的siRNA療法。該研究團(tuán)隊(duì)開發(fā)了針對(duì)脂滴表面蛋白PLIN2的GalNAc-siRNA偶聯(lián)藥物,并在多種脂肪肝病小鼠模型中驗(yàn)證了其顯著療效及良好的生物安全性。研究發(fā)現(xiàn),這種siRNA藥物可能通過(guò)促進(jìn)肝臟極低密度脂蛋白-甘油三酯(VLDL-TG)的分泌來(lái)發(fā)揮作用,并加速機(jī)體對(duì)分泌脂肪的代謝和產(chǎn)熱過(guò)程。此外,該siRNA藥物在野生型小鼠和人源化PLIN2敲入小鼠中均能有效緩解脂肪變性、炎癥和纖維化等多項(xiàng)指標(biāo),證實(shí)了其作為MASLD治療藥物的潛力。這項(xiàng)研究為脂肪肝病的治療提供了新的可能性,并為針對(duì)不同致病機(jī)制的患者群體提出了潛在的治療策略。
靶點(diǎn):USP52
應(yīng)用:膀胱癌研究
來(lái)源:Liu, Jianmin, et al. "Deubiquitylase USP52 Promotes Bladder Cancer Progression by Modulating Ferroptosis through Stabilizing SLC7A11/xCT." Advanced Science (2024): 2403995.
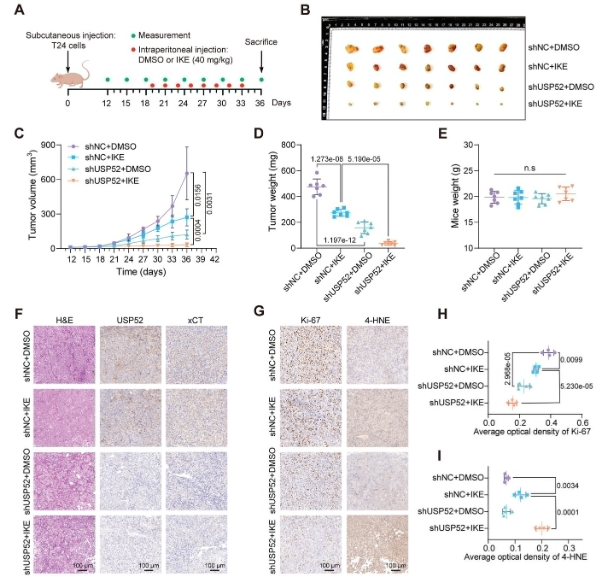
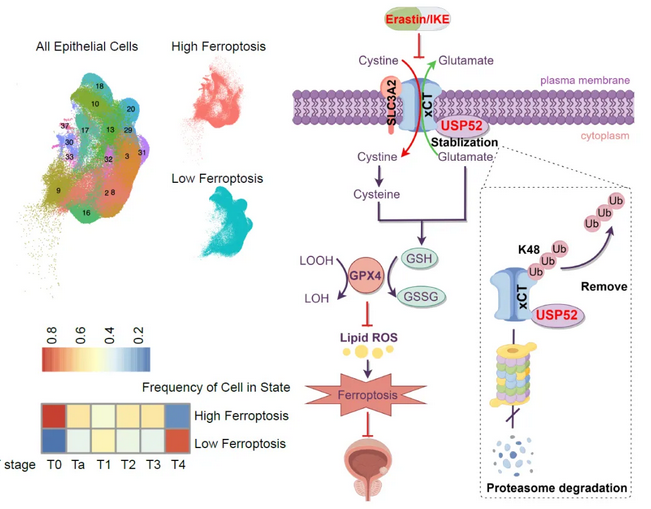
武漢大學(xué)中南醫(yī)院泌尿外科王行環(huán)教授團(tuán)隊(duì)在《Advanced Science》期刊上發(fā)表的研究成果揭示了去泛素化酶USP52通過(guò)穩(wěn)定SLC7A11/xCT蛋白調(diào)節(jié)鐵死亡敏感性,促進(jìn)膀胱癌的進(jìn)展。鐵死亡是一種由鐵依賴的脂質(zhì)過(guò)氧化引起的細(xì)胞程序性死亡方式,而System xc–/GSH/GPX4是主要的抗氧化防線。該研究發(fā)現(xiàn),膀胱癌細(xì)胞的鐵死亡狀態(tài)與膀胱癌分期呈負(fù)相關(guān),表明鐵死亡可能在膀胱癌發(fā)生中起抑制作用。通過(guò)siRNA文庫(kù)篩選和實(shí)驗(yàn)驗(yàn)證,研究團(tuán)隊(duì)發(fā)現(xiàn)USP52能夠穩(wěn)定xCT蛋白,抑制膀胱癌細(xì)胞的鐵死亡過(guò)程。敲減USP52可以增加細(xì)胞內(nèi)脂質(zhì)過(guò)氧化水平和亞鐵離子含量,增強(qiáng)細(xì)胞對(duì)鐵死亡的敏感性,從而抑制膀胱癌的進(jìn)展。臨床上,USP52在膀胱癌組織中的高表達(dá)與患者預(yù)后負(fù)相關(guān)。這項(xiàng)研究不僅闡明了USP52調(diào)控xCT影響鐵死亡抑制膀胱癌進(jìn)展的機(jī)制,還為膀胱癌患者的臨床精準(zhǔn)治療提供了新的思路和策略。
靶點(diǎn):SMURF1
應(yīng)用:溶酶體相關(guān)疾病的研究
來(lái)源:Xia, Qin, et al. "SMURF1 mediates damaged lysosomal homeostasis by ubiquitinating PPP3CB to promote the activation of TFEB." Autophagy just-accepted (2024).
北京理工大學(xué)生命學(xué)院董磊教授團(tuán)隊(duì)在《Autophagy》期刊上發(fā)表的研究揭示了SMURF1蛋白在維持細(xì)胞穩(wěn)態(tài)中的關(guān)鍵作用,特別是在促進(jìn)受損溶酶體自噬降解的過(guò)程中。研究團(tuán)隊(duì)發(fā)現(xiàn),SMURF1通過(guò)泛素化修飾PPP3CB蛋白,促進(jìn)受損溶酶體的自噬降解,這一過(guò)程對(duì)于細(xì)胞應(yīng)激響應(yīng)和溶酶體損傷后的修復(fù)至關(guān)重要。在溶酶體損傷后,PPP3CB作為橋梁,通過(guò)與LGALS3結(jié)合招募SMURF1,形成LGALS3-SMURF1-PPP3/calcineurin復(fù)合體,該復(fù)合體能夠穩(wěn)定TFEB,從而去磷酸激活TFEB并進(jìn)行溶酶體生成相關(guān)基因的表達(dá)。這一發(fā)現(xiàn)不僅增進(jìn)了我們對(duì)自噬過(guò)程分子機(jī)制的理解,而且為SMURF1作為治療應(yīng)激相關(guān)疾病的潛在藥物靶點(diǎn)提供了新的視角。該研究為開發(fā)新的治療策略提供了重要的基礎(chǔ),有助于未來(lái)針對(duì)溶酶體相關(guān)疾病的藥物設(shè)計(jì)和治療。
靶點(diǎn):VGLL3
應(yīng)用:腫瘤研究
來(lái)源:Wu, Wei, et al. "VGLL3 modulates chemosensitivity through promoting DNA double-strand break repair." Science Advances 10.41 (2024): eadr2643.

國(guó)家生物信息中心郭彩霞研究組與中國(guó)科學(xué)院動(dòng)物研究所唐鐵山研究組合作,在《Science Advances》期刊上發(fā)表了一項(xiàng)研究,揭示了VGLL3蛋白在調(diào)控腫瘤化療敏感性中的作用。研究發(fā)現(xiàn),VGLL3通過(guò)其N端的谷氨酸富集區(qū)和C端的組氨酸富集區(qū)促進(jìn)DNA雙鏈斷裂修復(fù),顯著影響腫瘤細(xì)胞對(duì)化療藥物的響應(yīng)。VGLL3能夠迅速被招募至DNA損傷部位,其招募依賴于多聚ADP-核糖化修飾介導(dǎo)的染色質(zhì)重塑。VGLL3的敲低或敲除能抑制腫瘤細(xì)胞的同源重組修復(fù),增強(qiáng)腫瘤細(xì)胞對(duì)多種化療藥物的敏感性。此外,VGLL3還能通過(guò)抑制關(guān)鍵蛋白CtIP和MDC1的蛋白酶體依賴性降解,促進(jìn)DSB末端剪切和RNF8/168信號(hào)通路,增強(qiáng)DSB修復(fù)。小鼠移植瘤實(shí)驗(yàn)進(jìn)一步證實(shí),敲低VGLL3能抑制腫瘤生長(zhǎng)、增強(qiáng)化療敏感性。鑒于VGLL3在多種惡性腫瘤中的高表達(dá)與患者的不良預(yù)后相關(guān),VGLL3有望成為一個(gè)新的腫瘤治療靶點(diǎn),這項(xiàng)研究為深入理解VGLL3的生理功能和腫瘤治療抵抗提供了理論基礎(chǔ)。
靶點(diǎn):Cdk5
應(yīng)用:乳腺癌腦轉(zhuǎn)移研究
來(lái)源:Yuzhalin, Arseniy E., et al. "Astrocyte-induced Cdk5 expedites breast cancer brain metastasis by suppressing MHC-I expression to evade immune recognition." Nature Cell Biology (2024): 1-17.

美國(guó)德克薩斯大學(xué)MD安德森癌癥中心的Dihua Yu研究團(tuán)隊(duì)在《Nature Cell Biology》上發(fā)表的研究揭示了Cdk5在乳腺癌腦轉(zhuǎn)移(BrM)中的作用機(jī)制。研究發(fā)現(xiàn),大腦中的星形膠質(zhì)細(xì)胞能夠誘導(dǎo)乳腺癌BrM細(xì)胞中Cdk5的高表達(dá),Cdk5通過(guò)Irf2bp1-Stat1-importin α-Nlrc5信號(hào)通路抑制MHC-I分子的表達(dá),從而幫助腫瘤細(xì)胞逃避免疫系統(tǒng)的識(shí)別和攻擊。使用Cdk5抑制劑RSV單獨(dú)或與免疫檢查點(diǎn)抑制劑聯(lián)合治療可以顯著抑制小鼠模型中的BrM生長(zhǎng)。這些發(fā)現(xiàn)表明,Cdk5的激活對(duì)于乳腺癌腦轉(zhuǎn)移的發(fā)展至關(guān)重要,且靶向Cdk5可能成為提高腫瘤免疫療法效果和治療腦轉(zhuǎn)移腫瘤的新策略。研究還指出,Cdk5抑制劑能夠恢復(fù)MHC-I的表達(dá)并增強(qiáng)T細(xì)胞反應(yīng),為未來(lái)的臨床治療提供了理論基礎(chǔ)。這項(xiàng)研究為理解腦轉(zhuǎn)移的免疫逃避機(jī)制和開發(fā)新的治療策略提供了重要見解。
靶點(diǎn):USP11
應(yīng)用:阿爾茨海默病(AD)研究
來(lái)源:Guo, Yi, et al. "Targeting USP11 regulation by a novel lithium-organic coordination compound improves neuropathologies and cognitive functions in Alzheimer transgenic mice." EMBO Molecular Medicine (2024): 1-26.

貴州醫(yī)科大學(xué)譚俊教授團(tuán)隊(duì)與大連醫(yī)科大學(xué)附屬第一醫(yī)院李崧研究員合作,在《EMBO Molecular Medicine》雜志上發(fā)表了一項(xiàng)突破性研究,發(fā)現(xiàn)了一種全新的小分子USP11抑制劑IsoLiPro(尼布林),用于治療阿爾茨海默病(AD)。研究發(fā)現(xiàn),USP11的高表達(dá)會(huì)促進(jìn)tau蛋白的去泛素化和穩(wěn)定性,阻礙其正常清除,加速病理性聚集,導(dǎo)致AD小鼠認(rèn)知功能障礙。譚俊團(tuán)隊(duì)通過(guò)篩選優(yōu)化得到IsoLiPro,它能夠顯著降低USP11蛋白水平,增加tau蛋白泛素化,促進(jìn)其降解,改善AD病理和認(rèn)知損害。在3xTg-AD和5xFAD轉(zhuǎn)基因AD動(dòng)物模型中,尼布林顯著緩解了大腦中的病理變化,并改善了認(rèn)知功能障礙。此外,尼布林在長(zhǎng)期給藥過(guò)程中顯示出低毒性和良好的藥代學(xué)特征,為其臨床研究提供了基礎(chǔ)。這一發(fā)現(xiàn)為AD治療提供了新的靶點(diǎn)和策略。
靶點(diǎn):TMED10
應(yīng)用:冠狀病毒研究
來(lái)源:Liu, Lei, et al. "Coronavirus envelope protein activates TMED10-mediated unconventional secretion of inflammatory factors." Nature Communications 15.1 (2024): 8708.

清華大學(xué)藥學(xué)院張敏實(shí)驗(yàn)室在《Nature Communications》上發(fā)表的研究揭示了重癥冠狀病毒導(dǎo)致宿主過(guò)度炎癥反應(yīng)的分子機(jī)制。研究團(tuán)隊(duì)發(fā)現(xiàn),重癥冠狀病毒的包膜蛋白(E蛋白)是導(dǎo)致炎癥風(fēng)暴的關(guān)鍵致病因子,它通過(guò)與TMED10蛋白強(qiáng)烈互作激活非經(jīng)典分泌途徑(THU),加劇炎癥因子的釋放。這一發(fā)現(xiàn)不僅強(qiáng)調(diào)了非經(jīng)典分泌在高致病性病毒感染中的關(guān)鍵作用,還提出了E-TMED10相互作用作為潛在的治療靶點(diǎn)。此外,研究還發(fā)現(xiàn)孕酮類似物能有效抑制炎癥因子的分泌,為開發(fā)抗炎藥物提供了新思路,有助于降低重癥冠狀病毒的致死率。這項(xiàng)研究不僅增進(jìn)了我們對(duì)冠狀病毒致病機(jī)制的理解,也為未來(lái)疫情的防控提供了重要的科學(xué)依據(jù)。
靶點(diǎn):AQP4
應(yīng)用:眼科和神經(jīng)退行性疾病的治療研究
來(lái)源:Cao, Qiuchen, et al. "Transport of β-amyloid from brain to eye causes retinal degeneration in Alzheimer’s disease." Journal of Experimental Medicine 221.11 (2024).

南京醫(yī)科大學(xué)劉慶淮和肖明團(tuán)隊(duì)在《Journal of Experimental Medicine》上發(fā)表的研究揭示了阿爾茨海默病(AD)中Aβ蛋白從大腦到眼睛的轉(zhuǎn)運(yùn)導(dǎo)致視網(wǎng)膜退行性變化。研究發(fā)現(xiàn),AD患者和AD模型小鼠的眼部組織中Aβ沉積增多,主要集中在視網(wǎng)膜和視神經(jīng)的血管周圍間隙,并在眶周淋巴管中沉積。研究提出了三種腦眼轉(zhuǎn)運(yùn)Aβ的途徑:視神經(jīng)鞘膜-淋巴途徑、軸突間隙途徑和動(dòng)脈周圍間隙途徑。此外,研究還發(fā)現(xiàn)水通道蛋白4(AQP4)可能介導(dǎo)了Aβ從腦到眼的轉(zhuǎn)運(yùn),AQP4基因敲除小鼠的Aβ從腦到眼的轉(zhuǎn)運(yùn)速率減緩,表明眼類淋巴系統(tǒng)-視神經(jīng)鞘膜淋巴管途徑可能在清除視網(wǎng)膜Aβ中發(fā)揮關(guān)鍵作用。這些發(fā)現(xiàn)不僅為理解AD進(jìn)程中眼部Aβ的來(lái)源和去向提供了新見解,也為眼科和神經(jīng)退行性疾病的治療提供了新的靶點(diǎn)。
參考文獻(xiàn)
1. Wang, Yao, et al. "Therapeutic siRNA targeting PLIN2 ameliorates steatosis, inflammation, and fibrosis in steatotic liver disease models." Journal of Lipid Research 65.10 (2024): 100635.
2. Liu, Jianmin, et al. "Deubiquitylase USP52 Promotes Bladder Cancer Progression by Modulating Ferroptosis through Stabilizing SLC7A11/xCT." Advanced Science (2024): 2403995.
3. Xia, Qin, et al. "SMURF1 mediates damaged lysosomal homeostasis by ubiquitinating PPP3CB to promote the activation of TFEB." Autophagy just-accepted (2024).
4. Wu, Wei, et al. "VGLL3 modulates chemosensitivity through promoting DNA double-strand break repair." Science Advances 10.41 (2024): eadr2643.
5. Yuzhalin, Arseniy E., et al. "Astrocyte-induced Cdk5 expedites breast cancer brain metastasis by suppressing MHC-I expression to evade immune recognition." Nature Cell Biology (2024): 1-17.
6. Guo, Yi, et al. "Targeting USP11 regulation by a novel lithium-organic coordination compound improves neuropathologies and cognitive functions in Alzheimer transgenic mice." EMBO Molecular Medicine (2024): 1-26.
7. Liu, Lei, et al. "Coronavirus envelope protein activates TMED10-mediated unconventional secretion of inflammatory factors." Nature Communications 15.1 (2024): 8708.
8. Cao, Qiuchen, et al. "Transport of β-amyloid from brain to eye causes retinal degeneration in Alzheimer’s disease." Journal of Experimental Medicine 221.11 (2024).
應(yīng)用:脂肪肝病的治療研究
來(lái)源:Wang, Yao, et al. "Therapeutic siRNA targeting PLIN2 ameliorates steatosis, inflammation, and fibrosis in steatotic liver disease models." Journal of Lipid Research 65.10 (2024): 100635.

(圖源:GalNAc-siPlin2 治療可改善 HFD/HFr 飲食誘導(dǎo)的 MASH 小鼠的炎癥和纖維化 [1])
北京大學(xué)生命科學(xué)學(xué)院朱健和劉敏課題組在《Journal of Lipid Research》上發(fā)表的研究論文中,報(bào)道了一種靶向治療脂肪肝病的siRNA療法。該研究團(tuán)隊(duì)開發(fā)了針對(duì)脂滴表面蛋白PLIN2的GalNAc-siRNA偶聯(lián)藥物,并在多種脂肪肝病小鼠模型中驗(yàn)證了其顯著療效及良好的生物安全性。研究發(fā)現(xiàn),這種siRNA藥物可能通過(guò)促進(jìn)肝臟極低密度脂蛋白-甘油三酯(VLDL-TG)的分泌來(lái)發(fā)揮作用,并加速機(jī)體對(duì)分泌脂肪的代謝和產(chǎn)熱過(guò)程。此外,該siRNA藥物在野生型小鼠和人源化PLIN2敲入小鼠中均能有效緩解脂肪變性、炎癥和纖維化等多項(xiàng)指標(biāo),證實(shí)了其作為MASLD治療藥物的潛力。這項(xiàng)研究為脂肪肝病的治療提供了新的可能性,并為針對(duì)不同致病機(jī)制的患者群體提出了潛在的治療策略。
靶點(diǎn):USP52
應(yīng)用:膀胱癌研究
來(lái)源:Liu, Jianmin, et al. "Deubiquitylase USP52 Promotes Bladder Cancer Progression by Modulating Ferroptosis through Stabilizing SLC7A11/xCT." Advanced Science (2024): 2403995.

(圖源:USP52 的缺失可通過(guò)促進(jìn)體內(nèi)鐵死亡來(lái)抑制 BLCA 進(jìn)展 [2])
武漢大學(xué)中南醫(yī)院泌尿外科王行環(huán)教授團(tuán)隊(duì)在《Advanced Science》期刊上發(fā)表的研究成果揭示了去泛素化酶USP52通過(guò)穩(wěn)定SLC7A11/xCT蛋白調(diào)節(jié)鐵死亡敏感性,促進(jìn)膀胱癌的進(jìn)展。鐵死亡是一種由鐵依賴的脂質(zhì)過(guò)氧化引起的細(xì)胞程序性死亡方式,而System xc–/GSH/GPX4是主要的抗氧化防線。該研究發(fā)現(xiàn),膀胱癌細(xì)胞的鐵死亡狀態(tài)與膀胱癌分期呈負(fù)相關(guān),表明鐵死亡可能在膀胱癌發(fā)生中起抑制作用。通過(guò)siRNA文庫(kù)篩選和實(shí)驗(yàn)驗(yàn)證,研究團(tuán)隊(duì)發(fā)現(xiàn)USP52能夠穩(wěn)定xCT蛋白,抑制膀胱癌細(xì)胞的鐵死亡過(guò)程。敲減USP52可以增加細(xì)胞內(nèi)脂質(zhì)過(guò)氧化水平和亞鐵離子含量,增強(qiáng)細(xì)胞對(duì)鐵死亡的敏感性,從而抑制膀胱癌的進(jìn)展。臨床上,USP52在膀胱癌組織中的高表達(dá)與患者預(yù)后負(fù)相關(guān)。這項(xiàng)研究不僅闡明了USP52調(diào)控xCT影響鐵死亡抑制膀胱癌進(jìn)展的機(jī)制,還為膀胱癌患者的臨床精準(zhǔn)治療提供了新的思路和策略。
靶點(diǎn):SMURF1
應(yīng)用:溶酶體相關(guān)疾病的研究
來(lái)源:Xia, Qin, et al. "SMURF1 mediates damaged lysosomal homeostasis by ubiquitinating PPP3CB to promote the activation of TFEB." Autophagy just-accepted (2024).

(圖源:USP52敲減能夠通過(guò)促進(jìn)鐵死亡顯著抑制膀胱癌進(jìn)展 [3])
北京理工大學(xué)生命學(xué)院董磊教授團(tuán)隊(duì)在《Autophagy》期刊上發(fā)表的研究揭示了SMURF1蛋白在維持細(xì)胞穩(wěn)態(tài)中的關(guān)鍵作用,特別是在促進(jìn)受損溶酶體自噬降解的過(guò)程中。研究團(tuán)隊(duì)發(fā)現(xiàn),SMURF1通過(guò)泛素化修飾PPP3CB蛋白,促進(jìn)受損溶酶體的自噬降解,這一過(guò)程對(duì)于細(xì)胞應(yīng)激響應(yīng)和溶酶體損傷后的修復(fù)至關(guān)重要。在溶酶體損傷后,PPP3CB作為橋梁,通過(guò)與LGALS3結(jié)合招募SMURF1,形成LGALS3-SMURF1-PPP3/calcineurin復(fù)合體,該復(fù)合體能夠穩(wěn)定TFEB,從而去磷酸激活TFEB并進(jìn)行溶酶體生成相關(guān)基因的表達(dá)。這一發(fā)現(xiàn)不僅增進(jìn)了我們對(duì)自噬過(guò)程分子機(jī)制的理解,而且為SMURF1作為治療應(yīng)激相關(guān)疾病的潛在藥物靶點(diǎn)提供了新的視角。該研究為開發(fā)新的治療策略提供了重要的基礎(chǔ),有助于未來(lái)針對(duì)溶酶體相關(guān)疾病的藥物設(shè)計(jì)和治療。
靶點(diǎn):VGLL3
應(yīng)用:腫瘤研究
來(lái)源:Wu, Wei, et al. "VGLL3 modulates chemosensitivity through promoting DNA double-strand break repair." Science Advances 10.41 (2024): eadr2643.

(圖源:VGLL3 富含 E 和 H 的基序有助于腫瘤的發(fā)展 [4])
國(guó)家生物信息中心郭彩霞研究組與中國(guó)科學(xué)院動(dòng)物研究所唐鐵山研究組合作,在《Science Advances》期刊上發(fā)表了一項(xiàng)研究,揭示了VGLL3蛋白在調(diào)控腫瘤化療敏感性中的作用。研究發(fā)現(xiàn),VGLL3通過(guò)其N端的谷氨酸富集區(qū)和C端的組氨酸富集區(qū)促進(jìn)DNA雙鏈斷裂修復(fù),顯著影響腫瘤細(xì)胞對(duì)化療藥物的響應(yīng)。VGLL3能夠迅速被招募至DNA損傷部位,其招募依賴于多聚ADP-核糖化修飾介導(dǎo)的染色質(zhì)重塑。VGLL3的敲低或敲除能抑制腫瘤細(xì)胞的同源重組修復(fù),增強(qiáng)腫瘤細(xì)胞對(duì)多種化療藥物的敏感性。此外,VGLL3還能通過(guò)抑制關(guān)鍵蛋白CtIP和MDC1的蛋白酶體依賴性降解,促進(jìn)DSB末端剪切和RNF8/168信號(hào)通路,增強(qiáng)DSB修復(fù)。小鼠移植瘤實(shí)驗(yàn)進(jìn)一步證實(shí),敲低VGLL3能抑制腫瘤生長(zhǎng)、增強(qiáng)化療敏感性。鑒于VGLL3在多種惡性腫瘤中的高表達(dá)與患者的不良預(yù)后相關(guān),VGLL3有望成為一個(gè)新的腫瘤治療靶點(diǎn),這項(xiàng)研究為深入理解VGLL3的生理功能和腫瘤治療抵抗提供了理論基礎(chǔ)。
靶點(diǎn):Cdk5
應(yīng)用:乳腺癌腦轉(zhuǎn)移研究
來(lái)源:Yuzhalin, Arseniy E., et al. "Astrocyte-induced Cdk5 expedites breast cancer brain metastasis by suppressing MHC-I expression to evade immune recognition." Nature Cell Biology (2024): 1-17.

(圖源:DOI: 10.1038/s41556-024-01509-5 [5])
美國(guó)德克薩斯大學(xué)MD安德森癌癥中心的Dihua Yu研究團(tuán)隊(duì)在《Nature Cell Biology》上發(fā)表的研究揭示了Cdk5在乳腺癌腦轉(zhuǎn)移(BrM)中的作用機(jī)制。研究發(fā)現(xiàn),大腦中的星形膠質(zhì)細(xì)胞能夠誘導(dǎo)乳腺癌BrM細(xì)胞中Cdk5的高表達(dá),Cdk5通過(guò)Irf2bp1-Stat1-importin α-Nlrc5信號(hào)通路抑制MHC-I分子的表達(dá),從而幫助腫瘤細(xì)胞逃避免疫系統(tǒng)的識(shí)別和攻擊。使用Cdk5抑制劑RSV單獨(dú)或與免疫檢查點(diǎn)抑制劑聯(lián)合治療可以顯著抑制小鼠模型中的BrM生長(zhǎng)。這些發(fā)現(xiàn)表明,Cdk5的激活對(duì)于乳腺癌腦轉(zhuǎn)移的發(fā)展至關(guān)重要,且靶向Cdk5可能成為提高腫瘤免疫療法效果和治療腦轉(zhuǎn)移腫瘤的新策略。研究還指出,Cdk5抑制劑能夠恢復(fù)MHC-I的表達(dá)并增強(qiáng)T細(xì)胞反應(yīng),為未來(lái)的臨床治療提供了理論基礎(chǔ)。這項(xiàng)研究為理解腦轉(zhuǎn)移的免疫逃避機(jī)制和開發(fā)新的治療策略提供了重要見解。
靶點(diǎn):USP11
應(yīng)用:阿爾茨海默病(AD)研究
來(lái)源:Guo, Yi, et al. "Targeting USP11 regulation by a novel lithium-organic coordination compound improves neuropathologies and cognitive functions in Alzheimer transgenic mice." EMBO Molecular Medicine (2024): 1-26.

(圖源:IsoLiPro可顯著降低 SH-SY5Y 細(xì)胞和小鼠大腦中的 USP11 蛋白水平 [6])
貴州醫(yī)科大學(xué)譚俊教授團(tuán)隊(duì)與大連醫(yī)科大學(xué)附屬第一醫(yī)院李崧研究員合作,在《EMBO Molecular Medicine》雜志上發(fā)表了一項(xiàng)突破性研究,發(fā)現(xiàn)了一種全新的小分子USP11抑制劑IsoLiPro(尼布林),用于治療阿爾茨海默病(AD)。研究發(fā)現(xiàn),USP11的高表達(dá)會(huì)促進(jìn)tau蛋白的去泛素化和穩(wěn)定性,阻礙其正常清除,加速病理性聚集,導(dǎo)致AD小鼠認(rèn)知功能障礙。譚俊團(tuán)隊(duì)通過(guò)篩選優(yōu)化得到IsoLiPro,它能夠顯著降低USP11蛋白水平,增加tau蛋白泛素化,促進(jìn)其降解,改善AD病理和認(rèn)知損害。在3xTg-AD和5xFAD轉(zhuǎn)基因AD動(dòng)物模型中,尼布林顯著緩解了大腦中的病理變化,并改善了認(rèn)知功能障礙。此外,尼布林在長(zhǎng)期給藥過(guò)程中顯示出低毒性和良好的藥代學(xué)特征,為其臨床研究提供了基礎(chǔ)。這一發(fā)現(xiàn)為AD治療提供了新的靶點(diǎn)和策略。
靶點(diǎn):TMED10
應(yīng)用:冠狀病毒研究
來(lái)源:Liu, Lei, et al. "Coronavirus envelope protein activates TMED10-mediated unconventional secretion of inflammatory factors." Nature Communications 15.1 (2024): 8708.

(圖源:TMED10和冠狀病毒的包膜蛋白(E蛋白)-的相互作用是E誘導(dǎo)炎癥所必需的 [7])
清華大學(xué)藥學(xué)院張敏實(shí)驗(yàn)室在《Nature Communications》上發(fā)表的研究揭示了重癥冠狀病毒導(dǎo)致宿主過(guò)度炎癥反應(yīng)的分子機(jī)制。研究團(tuán)隊(duì)發(fā)現(xiàn),重癥冠狀病毒的包膜蛋白(E蛋白)是導(dǎo)致炎癥風(fēng)暴的關(guān)鍵致病因子,它通過(guò)與TMED10蛋白強(qiáng)烈互作激活非經(jīng)典分泌途徑(THU),加劇炎癥因子的釋放。這一發(fā)現(xiàn)不僅強(qiáng)調(diào)了非經(jīng)典分泌在高致病性病毒感染中的關(guān)鍵作用,還提出了E-TMED10相互作用作為潛在的治療靶點(diǎn)。此外,研究還發(fā)現(xiàn)孕酮類似物能有效抑制炎癥因子的分泌,為開發(fā)抗炎藥物提供了新思路,有助于降低重癥冠狀病毒的致死率。這項(xiàng)研究不僅增進(jìn)了我們對(duì)冠狀病毒致病機(jī)制的理解,也為未來(lái)疫情的防控提供了重要的科學(xué)依據(jù)。
靶點(diǎn):AQP4
應(yīng)用:眼科和神經(jīng)退行性疾病的治療研究
來(lái)源:Cao, Qiuchen, et al. "Transport of β-amyloid from brain to eye causes retinal degeneration in Alzheimer’s disease." Journal of Experimental Medicine 221.11 (2024).

(圖源:AQP4 影響腦到眼的傳輸速率并加劇腦源性 Aβ 誘導(dǎo)的視網(wǎng)膜損傷 [8])
南京醫(yī)科大學(xué)劉慶淮和肖明團(tuán)隊(duì)在《Journal of Experimental Medicine》上發(fā)表的研究揭示了阿爾茨海默病(AD)中Aβ蛋白從大腦到眼睛的轉(zhuǎn)運(yùn)導(dǎo)致視網(wǎng)膜退行性變化。研究發(fā)現(xiàn),AD患者和AD模型小鼠的眼部組織中Aβ沉積增多,主要集中在視網(wǎng)膜和視神經(jīng)的血管周圍間隙,并在眶周淋巴管中沉積。研究提出了三種腦眼轉(zhuǎn)運(yùn)Aβ的途徑:視神經(jīng)鞘膜-淋巴途徑、軸突間隙途徑和動(dòng)脈周圍間隙途徑。此外,研究還發(fā)現(xiàn)水通道蛋白4(AQP4)可能介導(dǎo)了Aβ從腦到眼的轉(zhuǎn)運(yùn),AQP4基因敲除小鼠的Aβ從腦到眼的轉(zhuǎn)運(yùn)速率減緩,表明眼類淋巴系統(tǒng)-視神經(jīng)鞘膜淋巴管途徑可能在清除視網(wǎng)膜Aβ中發(fā)揮關(guān)鍵作用。這些發(fā)現(xiàn)不僅為理解AD進(jìn)程中眼部Aβ的來(lái)源和去向提供了新見解,也為眼科和神經(jīng)退行性疾病的治療提供了新的靶點(diǎn)。
參考文獻(xiàn)
1. Wang, Yao, et al. "Therapeutic siRNA targeting PLIN2 ameliorates steatosis, inflammation, and fibrosis in steatotic liver disease models." Journal of Lipid Research 65.10 (2024): 100635.
2. Liu, Jianmin, et al. "Deubiquitylase USP52 Promotes Bladder Cancer Progression by Modulating Ferroptosis through Stabilizing SLC7A11/xCT." Advanced Science (2024): 2403995.
3. Xia, Qin, et al. "SMURF1 mediates damaged lysosomal homeostasis by ubiquitinating PPP3CB to promote the activation of TFEB." Autophagy just-accepted (2024).
4. Wu, Wei, et al. "VGLL3 modulates chemosensitivity through promoting DNA double-strand break repair." Science Advances 10.41 (2024): eadr2643.
5. Yuzhalin, Arseniy E., et al. "Astrocyte-induced Cdk5 expedites breast cancer brain metastasis by suppressing MHC-I expression to evade immune recognition." Nature Cell Biology (2024): 1-17.
6. Guo, Yi, et al. "Targeting USP11 regulation by a novel lithium-organic coordination compound improves neuropathologies and cognitive functions in Alzheimer transgenic mice." EMBO Molecular Medicine (2024): 1-26.
7. Liu, Lei, et al. "Coronavirus envelope protein activates TMED10-mediated unconventional secretion of inflammatory factors." Nature Communications 15.1 (2024): 8708.
8. Cao, Qiuchen, et al. "Transport of β-amyloid from brain to eye causes retinal degeneration in Alzheimer’s disease." Journal of Experimental Medicine 221.11 (2024).










